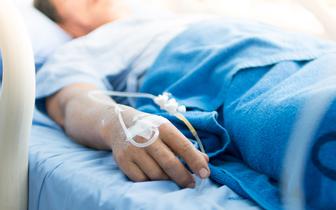
GIF wstrzymuje w obrocie lek kardiologiczny. Powodem działania niepożądane
Główny Inspektorat Farmaceutyczny podjął decyzję o wstrzymaniu na terenie całej Polski obrotu produktem leczniczym Qutiro 5mg/100ml, tirofiban (jako chlorowodorek tirofibanu).

Główny Inspektorat Farmaceutyczny wstrzymał na terenie całej Polski obrót produktem leczniczym o nazwie Qutiro 5mg/100ml, tirofiban (jako chlorowodorek tirofibanu) w infuzji 5 mg/ 100 ml, opakowanie 100 ml
Podmiot odpowiedzialny to QUESTUS PHARMA PRIVATE LIMITED z siedzibą w Indiach. Podmiot, który uzyskał zgodę na czasowe dopuszczenie leku do obrotu to Genesis Pharm sp. z o.o. sp. komandytowa.
U pacjentów po podaniu leku wystąpiły działania niepożądane
Do GIF wpłynęło od Wojewódzkiego Inspektora Farmaceutycznego w Opolu zgłoszenie podejrzenia wystąpienia wady jakościowej.
- Zgłoszone podejrzenie polegało na tym, że u pięciu pacjentów w jednym ze szpitali po wlewie produktu leczniczego Qutiro wystąpiły dreszcze oraz ból w klatce piersiowej. W posiewach krwi u tych pacjentów wyhodowano Klebsiella Pneumoniae ESBL. W szpitalu wykonano badania czystości mikrobiologicznej w zakresie higieny rąk personelu oraz badania ze środowiska: powierzchnie sprzętów, narzędzi, materiałów. W wykonanych posiewach nie wykazano obecności Klebsiella Pneumoniae. Na tej podstawie uznano, że istnieje podejrzenie niespełniania wymagań jakościowych produktu leczniczego Qutiro 5mg/100ml – informuje GIF.
Jak informuje GIF, w innym szpitalu po podaniu leku także stwierdzono działania niepożądane u trzech pacjentów.
Jak wskazał GIF, zasadne są wątpliwości, że występujące działania niepożądane u pacjentów po podaniu produktu leczniczego, "uzasadniają podejrzenie wystąpienia nieprawidłowości w zakresie jakości tego produktu leczniczego".
- Dodatkowo czynności wyjaśniające i weryfikujące podjęte przez personel szpitala, tj. wykonane posiewy krwi pacjentów, w których stwierdzono obecność bakterii Klebsiella Pneumoniae ESBL oraz to, że badania czystości mikrobiologicznej w zakresie higieny rąk personelu, badania ze środowiska: powierzchnie sprzętów, narzędzi, materiałów nie wykazały obecności bakterii Klebsiella Pneumoniae ESBL stanowią dodatkową okoliczność, wskazującą na potencjalny defekt jakościowy produktu leczniczego – informuje GIF.
PRZECZYTAJ TAKŻE: W 2023 r. EMA dopuściła do obrotu 77 produktów leczniczych stosowanych u ludzi. Ile z nich zawierało nową substancję czynną?
Źródło: Puls Farmacji

![Otyłe dzieci dwukrotnie częściej zapadają na stwardnienie rozsiane [BADANIA]](https://images.pb.pl/filtered/b6b9c5ca-d5af-44d2-9484-a2ebf1ce51e7/e5ac6b6f-0e1e-50e8-bcc6-72f61f06b1c8_xc_l.jpg)



![W Europie zanieczyszczenia powietrza powodują 800 tys. zgonów rocznie [WIDEO]](https://images.pb.pl/filtered/84b29d13-0727-4f42-8b21-de9566273376/76b0a951-3dc2-5503-975c-34480424e917_xc_l.jpg)
![Szansa na poprawę jakości życia dla pacjentów z HS [WIDEO]](https://images.pb.pl/filtered/08d54b79-36f0-499d-9e5e-731b6fdc1725/5e01a470-0cd4-51a2-9c4e-afeee2fc55b0_xc_l.png)