FDA zatwierdziła molnupiravir. To drugi lek do walki z COVID-19 dopuszczony w USA w ciągu tygodnia
Amerykańska Agencja Żywności i Leków (FDA) zatwierdziła do stosowania w trybie nadzwyczajnym doustną tabletkę molnupiravir - firmy Merck&Co. Wcześniej Agencja dopuściła do użytku Paxlovid firmy Pfizer. Oba leki powstały z myślą o osobach z grupy wysokiego ryzyka.
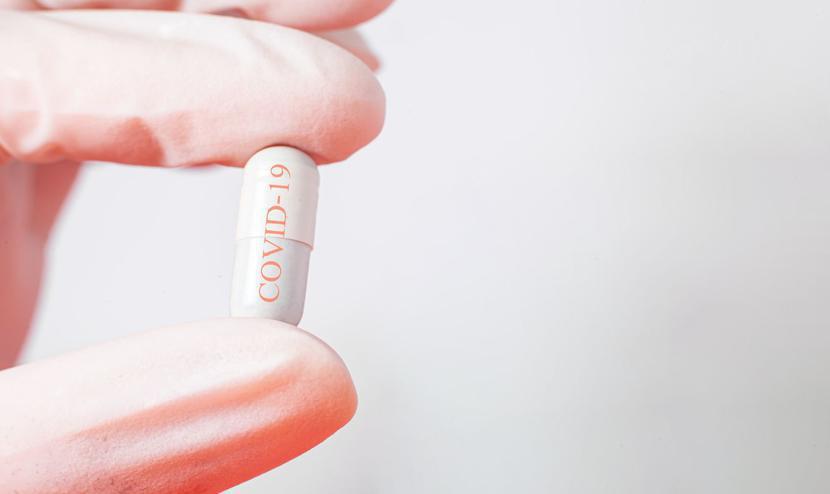
Molnupiravir zmniejsza ryzyko zgonu
FDA molnupiravir zatwierdziła w czwartek - 23 grudnia - do stosowania w trybie nadzwyczajnym do leczenia COVID-19 u dorosłych pacjentów z grup wysokiego ryzyka.
Lek firmy Merck w badaniu klinicznym, przeprowadzonym na osobach obarczonych wysokim ryzykiem na wczesnym etapie choroby, wykazał zmniejszenie liczby hospitalizacji i zgonów o około 30 proc. Przeznaczony jest do leczenia łagodnego do umiarkowanego przebiegu COVID-19 u dorosłych, u których występuje ryzyko ciężkiej choroby i dla których alternatywne metody leczenia nie są dostępne lub klinicznie nieodpowiednie.
Dwa leki dopuszczone w USA w ciągu tygodnia
W środę FDA dopuściła w trybie nadzwyczajnym do użytku Paxlovid, opracowany przez koncern Pfizer lek przeciwko COVID-19. Został on dopuszczony do stosowania u pacjentów w początkowym stadium choroby i nie jest przeznaczony dla osób hospitalizowanych czy jako środek zapobiegawczy lub zamiennik szczepionki.
Zdaniem FDA zarówno tabletki Merck, jak i Pfizera mogą być obiecującymi narzędziami dla osób chorych na COVID-19, zwłaszcza w obliczu szybko rozprzestrzeniającego się wariantu Omikron, który obecnie dominuje w Stanach Zjednoczonych.
– Ten lek jest również niezwykle łatwy w użyciu – powiedział Nick Kartsonis, wiceprezes Merck ds. badań klinicznych nad chorobami zakaźnymi.
Dodał: Nie wymaga żadnego drugiego leku, aby zwiększyć jego skuteczność, i można go podawać różnym specjalnym grupom pacjentów, w tym osobom, które mają poważne problemy z czynnością wątroby lub nerek. Nie trzeba przy tym martwić się o współdziałanie z towarzyszącymi lekami.
Kartsonis podkreślił, że lek pomaga zapobiegać replikacji wirusa i powinien być skuteczny przeciwko każdemu wariantowi, w tym Omikronowi.
Molnupiravir może blokować rozwój kości
FDA wyjaśniła, że lek firmy Merck nie jest dopuszczony do stosowania u pacjentów w wieku poniżej 18 lat, ponieważ jego składniki mogą wpływać na wzrost kości i chrząstki. Pigułka nie jest także zalecana do stosowania w czasie ciąży.
Lek ma być przyjmowany dwa razy dziennie – cztery tabletki za każdym razem, przez pięć dni, co daje pełny cykl leczenia 40 tabletkami. Według firmy Merck rząd USA złożył zamówienie na 3 mln tabletek.
PRZECZYTAJ TAKŻE: Molnupiravir będzie skuteczny na każdy wariant koronawirusa?
EMA wydała rekomendacje ws. trzech leków na COVID-19
Są rekomendacje EMA ws. stosowania molnupirawiru, ale lek nie został jeszcze dopuszczony do obrotu
EMA dokona przeglądu danych dot. skuteczności molnupirawiru w leczeniu COVID-19
Źródło: Puls Farmacji




![W Europie zanieczyszczenia powietrza powodują 800 tys. zgonów rocznie [WIDEO]](https://images.pb.pl/filtered/84b29d13-0727-4f42-8b21-de9566273376/76b0a951-3dc2-5503-975c-34480424e917_xc_l.jpg)
![Szansa na poprawę jakości życia dla pacjentów z HS [WIDEO]](https://images.pb.pl/filtered/08d54b79-36f0-499d-9e5e-731b6fdc1725/5e01a470-0cd4-51a2-9c4e-afeee2fc55b0_xc_l.png)



![Produkty bogate we flawonoidy zmniejszają ryzyko demencji [BADANIA]](https://images.pb.pl/filtered/19496e3b-993e-426c-b74c-1799e15f9041/8d1fb328-2b2f-5dc8-9983-bcb50569c2d5_mc_4.jpg)


