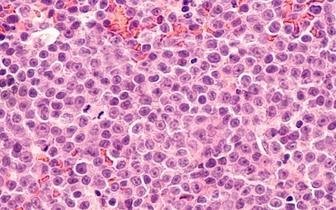
Nowy lek dla chorych na ostrą białaczkę szpikową
Amerykańska Agencja ds. Żywności i Leków zatwierdziła glasdegib (Daurismo, Pfizer) do stosowania w połączeniu z niskodawkową cytarabiną (LDAC) u pacjentów od 75. roku życia ze świeżo zdiagnozowaną ostrą białaczką szpikową (AML) lub cierpiących na inne chroniczne schorzenia lub choroby współistniejące, które mogą uniemożliwić stosowanie intensywnej chemioterapii.
"Intensywna chemioterapia jest zwykle stosowana do kontrolowania AML, ale wielu dorosłych nie może być nią leczona z powodu jej toksyczności. Dzisiejsza aprobata daje podmiotom zapewniajacym opiekę zdrowotną kolejne narzędzie do leczenia pacjentów z ostrą białaczką szpikową o różnych, unikalnych potrzebach. Badania kliniczne wykazały, że przy użyciu Daurismo w połączeniu z LDAC całkowite przeżycie zostało poprawione w porównaniu do LDAC dla pacjentów, którzy nie tolerują intensywnej chemioterapii” – powiedział dr Richard Pazdur, dyrektor Oncology Center of Excellence w Food and Drug Administration.
Skuteczność nowego leku badano w randomizowanym badaniu klinicznym, w którym 111 dorosłych pacjentów z nowo zdiagnozowaną AML leczono nim w połączeniu z niskodawkową cytarabiną lub samą chemioterapią. Mierzono w nim całkowity czas przeżycia (OS) od momentu randomizacji do śmierci z dowolnej przyczyny. Wyniki wykazały znaczną poprawę OS u pacjentów leczonych Daurismo w połączeniu z LDAC – mediana OS wyniosła u nich 8,3 miesiąca w porównaniu z 4,3 miesiąca w przypadku pacjentów leczonych wyłącznie LDAC.
Do częstych działań niepożądanych zgłaszanych przez pacjentów otrzymujących glasdebig w badaniach klinicznych należały: niedokrwistość, zmęczenie, krwawienie, neutropenia z gorączką, ból mięśni, nudności, obrzęk ramion lub nóg, małopłytkowość, duszność, zmniejszony apetyt, zaburzenia smaku, zapalenie błony śluzowej jamy ustnej lub gardła, zaparcia i wysypka.
Źródło: Puls Medycyny
Podpis: MMD





![W Europie zanieczyszczenia powietrza powodują 800 tys. zgonów rocznie [WIDEO]](https://images.pb.pl/filtered/84b29d13-0727-4f42-8b21-de9566273376/76b0a951-3dc2-5503-975c-34480424e917_xc_l.jpg)
![Szansa na poprawę jakości życia dla pacjentów z HS [WIDEO]](https://images.pb.pl/filtered/08d54b79-36f0-499d-9e5e-731b6fdc1725/5e01a470-0cd4-51a2-9c4e-afeee2fc55b0_xc_l.png)